土壤中铜过量的综述及修复技术
铜是植物生长发育所必需的微量营养元素。适量的铜可促进植物的正常生长和发育,在植物的生理代谢中起着重要的作用。但铜也是重金属元素,当土壤中铜含量超过土壤自净能力时,铜会积累在土壤中,甚至造成土壤污染。有研究表明,土壤中铜的缺乏和过剩都会对植物生长发育造成影响。
一、铜的来源
土壤中Cu 的来源有自然成土因素和人为因素两种。自然成土因素包括母质中矿物的风化、铁锰沉淀等作用,而人为因素主要是化肥、农药、污泥和禽畜粪便、废水灌溉、大气沉降物等。
二、土壤中铜含量及成土母质的影响
Cu 在自然界中分布广泛,但含量很低。通常情况下,Cu 在非污染土壤和沉积物中为20-30 mg/kg,非污染自然水体中低于2μg/L,植物体内的含量一般为10-100 mg/kg,主要分布在植物幼嫩部分。

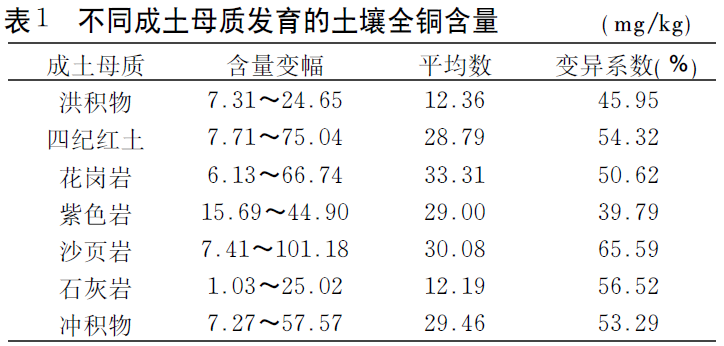
土壤全铜含量的高低,主要受成土母质及成土条件的影响。成土母质不同,土壤全铜含量有明显差异。花岗岩发育的土壤全铜含量最高,平均为33.31mg/kg;其次是沙页岩发育的土壤,为30.08mg/kg;石灰岩发育的土壤全铜含量最低,平均仅为12.19mg/kg。
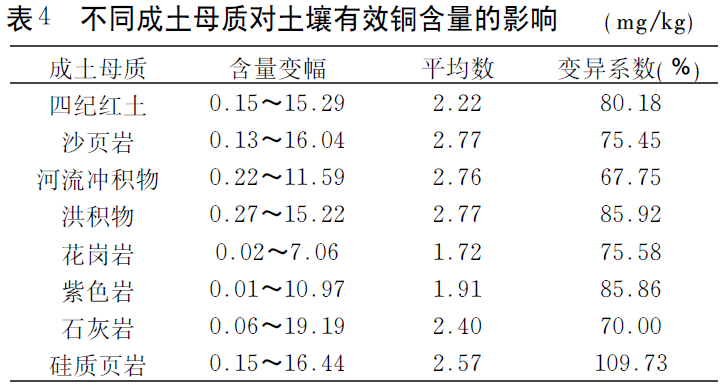
在各类耕地土壤中,不同成土母质发育的土壤有效铜含量有所不同。土壤有效铜含量从高到低的排序为:沙页岩、洪积物>河流冲积物>硅质页岩>石灰岩>四纪红土>紫色岩>花岗岩。

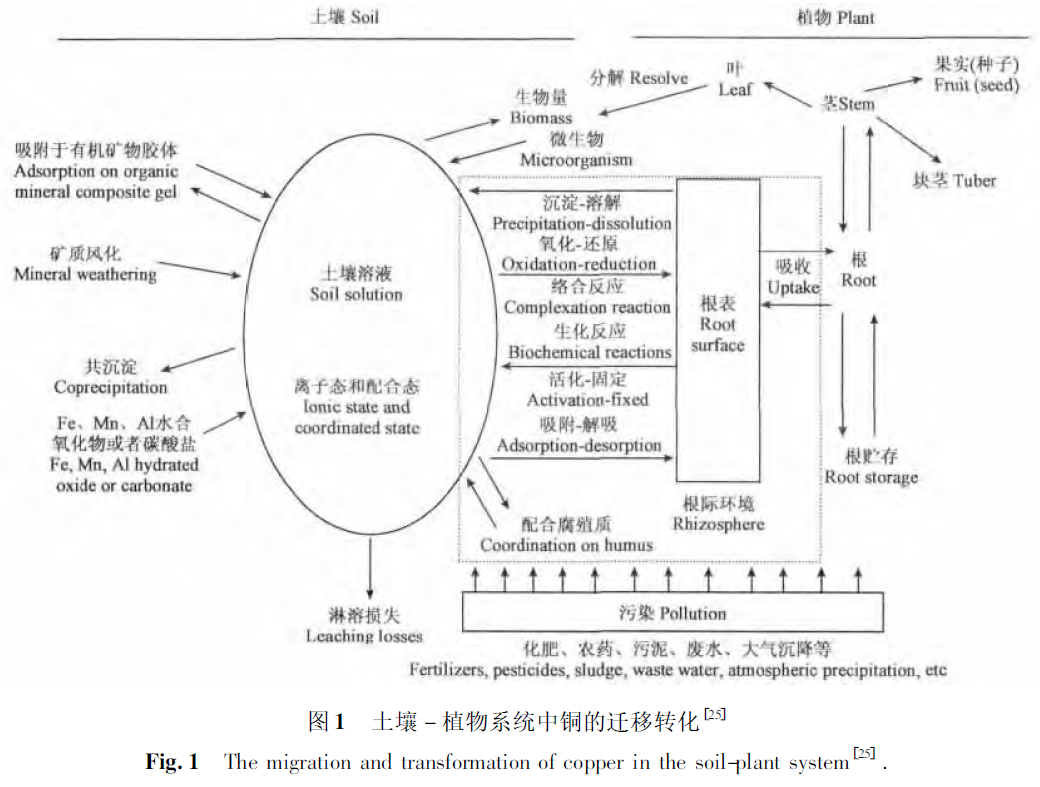
三、土壤中铜的存在形式及转化
土壤中铜的化学形态一般分为水溶态、交换态、碳酸盐结合态、铁锰氧化物结合态、有机结合态和残留态,大量研究证明,水溶态和交换态属于有效态或可给态,是植物吸收的主要形态。植物通过根部从土壤中以离子形式吸收铜,也可以通过叶面吸收。植物根系主要吸收二价铜离子。土壤溶液中铜离子浓度很低,离子与各种配位体有很强的亲和力,形成的螯合态铜也可能被植物吸收,在木质部和韧皮部也以螯合态转运。张维碟等的研究表明各结合形态铜的植物可利用性顺序是:水溶交换态>有机结合态>碳酸盐结合态>铁锰氧化物结合态>残渣态。上述形态的铜在一定条件下可以互相转化,每种物质含量的多少受不同反应平衡常数的控制。
土壤溶液中主要以离子态和配合态形式存在,铜离子容易被土壤中的有机矿物胶体吸附、腐殖质配合和铁锰铝水合氧化物或者碳酸盐沉淀而固定,同时也会由微生物代谢作用、有机和矿物胶体的解吸作用而返回土壤溶液中。
陈家武等研究表明,玉米根际土壤中各种形态Cu 含量的顺序为:有机结合态> 铁锰氧化物结合态> 碳酸盐结合态> 交换态。种植作物以后,根际土壤中有机结合态变化不明显,但是交换性Cu 含量显著增加,而铁锰氧化态和碳酸盐结合态Cu 含量减少;而且Cu 形态的变化还与植物种类有关。
四、铜在土壤中的吸附方式
铜在土壤中有两种吸附方式,即交换吸附和专性吸附。一般来说,当土壤全铜含量小于100Cu2+mg/kg时,铜吸附首先发生在强吸附位点上,主要是专性吸附;当含量大于该值时,铜吸附发生在弱吸附位点,主要是交换吸附。被专性吸附的金属离子均非交换态,不能为通常提取交换性阳离子的提取剂提取,只能为亲和力更强的金属离子置代(或部分置代)。土壤胶体对铜离子的专性吸附作用,是影响土壤中铜生物有效性的主要因素。
土壤中重金属专性吸附的载体主要有Fe/Al氧化物、有机质和粘土矿物。土壤Fe/Al氧化物表面也存在结合能大小不同的吸附点,铜浓度低时,首先占据结合能很大的吸附点,这些吸附点所吸附的铜只能被酸解吸。粘土矿物对铜离子的专性吸附能力要比氧化物和有机质小,但它在土壤中的数量要比氧化物和有机质多,因此它也起着重要的作用。
植物从土壤溶液中吸取铜后,土壤溶液中的铜浓度不断由专性吸附的铜补充,这样,土壤胶体所吸附的铜有一部分会重新进入土壤溶液,被植物吸收。而结合能大吸附点所吸附的铜不易于解吸,同时该种吸附的吸附量不受土壤中铜浓度变化的影响。(德德沐农业)从土壤对外来重金属污染的缓冲作用和环境容量看,这种紧结合态铜起重要作用。因此,Fe/Al氧化物、有机质和相关粘土矿物含量高的土壤,有较高的重金属铜污染的缓冲能力。
铜与土壤中其它重金属共存,会发生协同作用、加和作用或拮抗作用,从而在一定程度上增强或减轻污染的危害。吴燕玉等所做的盆栽实验表明,Cd-As复合污染会导致苜蓿吸收更多的Cu、Pb。倪才英等的研究表明Fe2+、Zn2+与Cu2+的拮抗作用,而Mn2+与Cu2+有协同吸收作用。因此,Cu2+与Mn2+或者Cd-As复合污染的土壤会增强铜和相关重金属的污染程度。
五、土壤因子对铜活性的影响
1、土壤pH值对铜有效性的影响
pH 改变会导致土壤中重金属化学形态的变化,一般随着pH 的升高,重金属的有效性降低。Cu 在酸性土壤中移动性较强,多以水溶态或配合态存在,容易被植物吸收而产生毒害;在中性或碱性条件下,Cu 的移动性很差,多以碳酸盐和铁锰氧化结合态等作物难利用形态存在,不对植物体产生毒害。随着土壤pH 的升高,土壤胶体所带的负电荷逐渐增加,Cu 被结合得更加牢固,从而抑制了有效态Cu 向其他形态的转化。
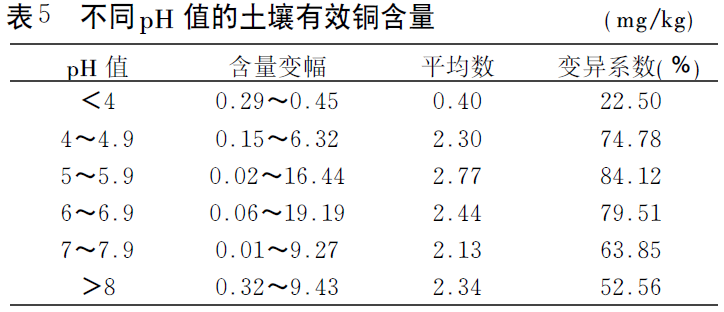
有研究发现,耕地土壤有效铜含量在pH 值为5~5.9的范围内最高,而当pH 值小于5时,土壤有效铜与土壤pH 值呈显著正相关,这是由于土壤在强酸性条件下,氧化铝的吸附及淋溶作用强烈,有效铜含量随pH 值的下降而减少。在pH 值大于6时,土壤有效铜与土壤pH 值呈负相关,表明随着pH 值的增加,铜的溶解度降低而使有效铜含量减少。
2、植物根际环境对铜有效性的影响
在植物根际环境中,根系对根际土壤中阴、阳离子选择性吸收以及根际养分胁迫等都会改变根际pH;同时微生物合成和植物根系分泌等产生的低分子量有机酸,以及它们代谢释放的CO2溶于土壤溶液,均会改变根际土壤的pH。这些原因导致根际土壤的pH 比非根际土壤低1-2 个单位。因此,通过沉淀- 溶解和吸附- 解吸等反应,Cu 会由铁锰氧化物结合态或者碳酸盐结合态向有效性较高的离子交换态、水溶态转化,从而使得根际土壤Cu 的活性比非根际土壤高。
3、土壤氧化还原电位(Eh) 的变化对重金属的影响
土壤Eh 的变化对重金属的沉淀—溶解平衡也有很大的影响。在还原条件下,土壤Eh 降至负值时,土壤中的含硫化合物生成H2S,可溶性铜大多生成难溶性CuS;相反,氧化状态下,Cu会由无效态向有效性较高的水溶态和交换态转化。根际土壤的Eh一般比非根际土壤低50 ~100 mV。根际Eh 改变时导致根际Cu 的形态变化,硫化物结合态Cu 在氧化条件下因硫被氧化,可能释放出其结合的Cu,从而造成有机结合态Cu 含量比例的下降;Cu2+被释放到根际环境中会向其他形态转化,如转化为酸可提取态和残渣态等。齐雁冰等研究表明,Cu的形态分布在不同Eh下有显著差异。在氧化状态下,Cu 的主要结合形态为残渣态,占43% 左右,其次为有机结合态和氧化物结合态,各占25% 左右,酸可提取态仅5% 左右。而在还原状态下,残渣态降低25%左右,氧化物结合态和有机结合态所占比例显著增加,成为主要形态,各占35% ~ 40%,酸可提取态所占比例仍然最低,但是所占比例明显降低至1%左右。
4、土壤有机质对铜形态的影响
土壤有机质直接影响土壤理化性状,制约土壤中Cu 的化学形态分布。水溶性有机质(dissolved organic matter,DOM) 移动性强,能够充当重金属的配位体和迁移载体,并且含有大量的功能基团。DOM 可以与Cu 发生络合和螯合等反应,使可交换态Cu 含量相对增多,提高Cu 的活性与迁移性,增加Cu 的有效性。
根际较强的微生物活动以及植物根系的作用,可导致根际土壤中的DOM 相对高于非根际土壤。
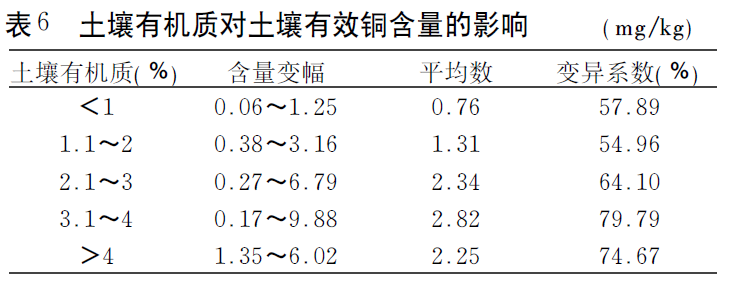
土壤中铜的结合形态主要是有机态铜。分析统计表明,在有机质含量<4%的土壤中,有机质含量与有效铜含量呈极显著的正相关,有效铜随有机质含量的增加而增加;在有机质含量>4%的土壤中,土壤中铜的有效性与有机质含量呈负相关,有效铜随有机质的增加而下降。(德德沐农业)这与土壤有机质在土壤中的腐解程度不同、腐殖质组成不同及其对铜络合的功能团和稳定性不同有关,有机质中的胡敏酸和富里酸可固定土壤中的铜离子,使铜的有效性降低。
土壤中的有机质主要为腐殖质。Schnitzer等指出,腐殖质中强酸性羧基与Cu2+离子形成的螯合物较稳定。腐殖质各个组分与铜络合或螯合后的有效性不一样。其中胡敏酸和胡敏素与铜离子形成的络合物不易解吸,而富里酸和铜离子形成的络合物则容易解吸。
在土壤铜含量较高时有机结合态、锰结合态的含量较高,以有机结合态的含量最高,有机质在这种土壤中成为铜缓冲的主要物质。其他的研究也认为有机质在土壤中是与铜结合的重要物质。
有研究说明施用有机肥能明显影响土壤中铜的存在形态,其规律是显著增加有机结合态铜的量,降低锰结合态铜的量。此外无定型铁结合态的组分也有降低的趋势,而交换态组分虽有增加的趋势,但在不同处理间差异未达显著水平,其它各组分无明显的变化规律。有机结合态铜含量的增加可能是因为施用有机肥增加了土壤中腐殖质的含量,从而对土壤中水溶态和交换态铜的络合增强,而水溶态和交换态铜含量的降低又促进了土壤中与矿物质结合态铜的溶解。另外作为一种弱酸,腐殖酸也能对土壤中难溶态铜有一定的溶解作用,在有机结合态铜增加的同时,与水溶性小分子富里酸结合部分的铜也会使铜的移动性有所增强。
5、根系分泌物对重金属形态的影响
根系分泌物能改变根际土壤的理化性质,影响植物的生长发育,同时可为土壤微生物提供能源,影响根际微生物的群落结构以及代谢活动。根系分泌物的成分比较复杂,除了根系细胞被动渗漏或主动释放到根际环境中的一些低分子量化合物质( 如H+、糖类、有机酸、酚类、氨基酸等),还包括一些由于根系细胞主动或者机械损伤被动释放的高分子量化合物质,如黏胶、外酶、植物络合素、类金属硫蛋白和植物高铁载体等,这些化合物能够螯合土壤重金属、酸化根际土壤,改变重金属的形态。根系分泌物中某些金属结合蛋白和特殊有机酸能螯合重金属。根分泌的粘胶物质与根际土壤中的Cu2+ 络合,形成稳定的螯合体,将其固定在污染土壤中。
6、微生物对重金属形态及有效性的影响
微生物在根际扮演着重要的角色,与土壤酶的种类、数量和生理活性等有极大的相关性,同时与重金属在根际环境中的迁移转化联系密切。根际微生物通过多种方式影响重金属的生化反应,包括改变土壤溶液pH、产生H2S、微生物铁载体和有机物种类,从而影响重金属的化学行为。微生物的细胞壁及粘液层可直接吸收固定重金属或分解代谢而重新将污染物释放到环境中,微生物代谢活动及产物也会加快矿物质的风化,进而影响重金属在根际的分布;此外,根际微生物也可通过改善土壤的团粒结构、改变根际环境理化性质和根系分泌物的组成等间接地作用于重金属,改变其形态和有效性。
根际微生物对Cu 的化学行为有很大影响,它们通过分泌有机酸、呼吸释放CO2等生理作用和生化反应来改变根际pH 和土壤对Cu 的吸附特征,进而改变Cu 在根际的存在形态和毒性。
六、铜元素对植物的影响
1、铜元素对植物的作用
铜(Cu)是植物生命活动必需的微量矿质元素,广泛参与各种生命活动。铜是植物生长发育必需的微量营养元素,它在调整蛋白质构成、参与光合作用、线粒体的呼吸作用和细胞壁的新陈代谢等方面起着重要作用。铜对植物正常的发育、产量、品质及生理代谢有着重要的影响。由于铜具有累积性会在植物体内累积,植物体内铜含量过高会影响植物正常的代谢功能,进而对植物的养分吸收、生长和产量、品质产生危害。
(1)铜是叶绿体的组成成分,铜大部分集中在叶绿体中,这些铜在叶绿体中形成类脂物质,对叶绿素及其他色素的合成和稳定起促进作用。另外,铜是叶绿体中质体蓝素的组成成分,质体蓝素是光合作用过程中电子的传递体。在光合作用系统中,铜通过本身化合价的变化,起电子传递作用。
(2)铜是某些氧化酶的组成成分,可促进作物呼吸作用和新陈代谢过程,农作物体内的一些酶,如多酚氧化酶、抗坏血酸氧化酶、细胞色素氧化酶、苯丙氨酸解氨酶、苯丙烷合成酶、乳酸氧化酶、脱氢多酸氧化酶等都是含铜的酶。这些酶的作用,一是促进作物呼吸作用的正常进行,二是促进农作物新陈代谢作用。
(3)铜是亚硝酸和次亚硝酸还原酶的活化剂,能促进农作物体内的硝酸还原作用。农作物从土壤中吸收的氮素,多数是硝态氮,硝态氮转化为铵态氮后,才能均衡形成组氨酸、赖氨酸、谷氨酸等,进一步促进蛋白质的合成。铜是亚硝酸和次亚硝酸还原成铵态氮不可缺少的元素。
(4)铜能增强农作物抗病害能力,主要机制:一是铜能促进作物细胞壁木质化,使病菌难以侵入作物体;二是铜能促进作物体内聚合物的合成,杜绝了病菌的营养源。
2、铜缺乏对植物的危害及症状
缺铜植株生长瘦弱,新生叶失绿发黄,呈凋萎干枯状,叶尖发白卷曲,叶缘黄灰色,叶片上出现坏死的斑点,分蘖或侧芽多,呈丛生状,繁殖器官的发育受阻。
(1)、禾本科作物:新叶呈灰绿色,卷曲、发黄,老叶在叶舌处弯曲或折断,叶尖枯萎,叶梢下部有灰白色斑点,有时扩展成条纹,并易感染霉菌性病害。麦类缺铜发生顶端黄化病,新叶黄白化,质薄、扭曲,后期上位叶子卷成纸捻状,轻度缺铜,前期症状不明显,抽穗后因花粉败育而不实一穗而不实。

(2)、豆类作物:新叶失绿、卷曲。豌豆花由鲜艳的红褐色变为暗淡的漂白色。
(3)、果树:叶片失绿畸形,嫩枝弯曲下垂,树皮上出现水泡状皮疹。严重时发生顶梢枯死,并逐渐向下发展,侧芽增多,树皮出现裂纹,并分泌出胶状物。果实小,果实变硬。柑橘叶片缺铜时新梢长而软,卷曲面“S”形,叶色暗绿,叶形变态,叶脉弯曲。
(4)、蔬菜:番茄缺铜侧枝生长缓慢,叶色呈深蓝绿色,叶卷缩。花发育受阻,不形成花。根系发育受阻。整常叶片含铜7-20μg/g,少于4μg/g为缺铜,少于1.7μg/g为严重缺铜。黄瓜缺铜生长受抑制,幼叶小,节间短,呈丛生状。后期叶片呈浓绿色到青铜色,症状从老叶向新叶发展。发育不良,影响开花,结果小,果实黄绿色,果皮上分散有小的凹陷斑。整常叶片含铜量7-17μg/g,低于4μg/g为缺铜。甜椒缺铜植株生长受阻,叶片变小,叶缘上卷。整常叶片含铜量6-20μg/g,少于4μg/g为缺铜。莴苣缺铜生长严重受阻,叶细小,叶片向下卷曲呈杯状。叶片黄化,沿叶柄和叶缘首先表现症状,从叶缘向里逐渐变黄,且从老叶向新叶发展。整常叶片含铜量5-15μg/g,少于2μg/g为缺铜。
3、铜过量对植物的危害及症状
近年来,含Cu 杀菌剂在农业生产过程中的长期频繁使用、畜牧业生产过程中含Cu 废物的农田施用、Cu 矿的开采和加工利用等都引起并加重了土壤环境的Cu 污染,使得Cu 污染已经成为重金属污染的重要方面之一。
过量铜胁迫将诱导植物细胞产生大量活性氧,引起膜脂过氧化,膜透性增大,细胞内容物大量外渗,甚至发生细胞死亡。
植物铜中毒会出现失绿症,主要是由缺铁引起的;另外铜毒害抑制光合电子转移,而且破坏光系统Ⅱ,导致作物光合作用及其产量下降。有研究表明,铜浓度高时,紫云英种子萌发期会出现胚轴畸形,变色腐烂;在生长发育期会生育迟缓,植株矮小,主根生长不良。杨桂芬等的研究表明,高浓度铜在水稻根部累积,会使水稻根系变粗,根毛变少,影响根系对养分的吸收,谷粒不饱满,造成减产。小麦遭受铜毒害,会出现生长前期的株高和分蘖受抑。
水培试验结果表明,铜毒害致使蔬菜植株矮小、原生根生长受抑制,新生根短、粗,根数少、根尖变褐;叶片失绿变黄;根长、根重、株高、生物量显著下降。不同蔬菜受害部位、受害程度不同,所有供试蔬菜中,大白菜对铜毒害最敏感,属于对铜的高敏感植物;豇豆对铜的耐性最强。
以大白菜为测试作物的土壤铜毒害试验结果表明,当向土壤添加铜大于200mg/kg时,大白菜全部黄化枯死;当向土壤添加铜60~60mg/kg时,大白菜生长基本停止;当向土壤添加铜5~60mg/kg时,随添加铜浓度的增加,大白菜根长、根重、根系活力、株高和生物量均逐渐下降。


许多研究表明钙、铁能缓解铜对植物的毒害作用。这是由于增加铁的使用可以大大减少进入植物体内的铜量,并使已进入植物根系的铜更多地分布在根部,从而减少了地上部铜的含量,减小铜的毒害。
铜在植物中的分配一般是地下部远大于地上部,由于不用植物对铜的吸收能力不同,其地上部在茎、叶和果实中的分配也不一样,一般是根>茎>叶。有的是叶>茎。
铜会影响种子萌发,降低种子的发芽率,抑制胚根生长。高浓度铜毒害会抑制细胞分裂,造成幼根颜色变褐变黑,生长不良,甚至停止生长,影响种子酶活性。使子叶发黄,种子鲜重下降。
郑曦等研究表明,在铜对种子的毒害中,当铜浓度大于80mg/kg时,会抑制小麦种子的萌发;铜浓度大于50 mg/L时,根生长受抑制,在铜浓度为300~500 mg/L时,根的生长停留在瘤状物阶段,呈焦黄或黑色;生长也受抑制,但抑制程度小于根。在种子萌发期间,紫云英在高铜胁迫下,胚轴畸形,根尖上翘、变色腐烂,最后会因生长点吸水困难而死亡。刘登义等研究表明铜会通过抑制植物种子萌发过程中蛋白酶、淀粉酶d的活性和呼吸强度,来降低贮存物质的分解速度,阻碍种子萌发所需要的物质和能量供应,从而使种子萌发率降低。在幼苗生长过程中,铜会抑制根尖细胞的有丝分裂、干扰酶促反应,从而抑制根的正常发育,对作物幼苗生长产生不良影响。(德德沐农业)刘文莉等在铜对腊梅种子毒害的试验也有类似的结果,高浓度铜抑制夏蜡梅种子萌发过程中的淀粉酶、蛋白酶和脂肪酶的活力,降低贮存物质的呼吸作用,并在萌发初期产生明显的抑制作用,从而抑制种子萌发。
高浓度铜会造成植物生长不良,植株矮小,叶片失绿,根生长受抑制,导致品质、产量下降。在莴苣定植两周后,酸性土施入大于100 mg/kg铜溶液,铜毒害导致莴苣植株矮小、叶片数少、小、老叶枯萎、嫩叶发黄、心叶呈蓝绿色等受害症状。刘春生等研究表明,褐土施加过量铜则会抑制苹果新梢的伸长和降低叶片中活性铁的含量,从而使叶绿素含量极显著的下降,施加高剂量铜的苹果叶片呈网纹状失绿,叶片黄色或黄白色,边缘褐色干枯,严重时部分叶片枯死。当铜浓度大于6mg/L时,紫云英叶片变黄,植株出现不同程度的弯曲、倒伏。
植物受铜毒害的最初部位是根。过量的铜积累于根部导致根尖细胞分裂受抑制,使生长受抑制,从而影响整个植株的生长。主要表现为主根生长不良,原生根呈褐色且粗短,根毛少。姚益云等研究表明,随土壤铜浓度增高,紫云英的根细胞结构遭破坏逐渐加重,具体特征为表皮层断裂、变褐,细胞壁变形,细胞质收缩、质壁分离,严重时细胞解体,壁内空腔,皮层、中柱细胞死亡,根吸收水分和养分能力降低,成活率低,甚至绝苗。朱云集等研究结果表明,随铜浓度的提高,小麦胚根、次生根数减少,根长、胚芽重也减少。陈桂珠也发现,Cu、Cd过量时,黄瓜根尖分生组织细胞质变薄,质壁分离,整个细胞呈松弛状态,这是由于Cu、Cd会干扰细胞质的生理代谢活动,从而影响有丝分裂的能量供应,导致根尖细胞分裂数减少,分裂速度减慢,造成根尖生长抑制。Leep研究发现,高浓度铜会导抑制根冠细胞分裂,根生长基本停止。Kahle认为这是铜导致分生区细胞核变小,核仁变小,阻滞了其分裂。而细胞有丝分裂指数有助于了解环境胁迫对植物生长的影响。
铜毒害会明显降低植株产量。由于高浓度铜抑制根系生长,降低根系活力,使叶绿素降低,导致养分吸收减少,光合速率降低,影响到植株产量和品质。刘景春等的研究表明,当铜浓度大于100mg/kg,辣椒的干重和产量分别下降了71.26%和71.16%。徐加宽等的研究也表明,当土壤铜浓度为100mg/kg时,水稻减产10.1%,并随土壤中铜浓度的升高而逐渐降低。
铜过量能明显降低植物叶片的叶绿素,使叶片失绿,变黄,光合作用下降。铜胁迫降低光合作用主要原因是,铜胁迫能明显降低植株叶片光合色素含量,破坏内囊体膜结构,修饰加工色素分子和降低色素合成酶的活性等,从而降低植物光合作用效率 。铜胁迫还会抑制和妨碍叶绿素进入光合系统。
铜胁迫导致植物细胞膜结构和功能遭到了破坏。铜胁迫会导致植物细胞摸透性增大,其氧化产物MDA含量增加,电导率增大,影响植物生长。这主要是因为铜与氧结合易产生超氧阴离子,而在中性水相环境中,超氧阴离子可转化为H2O2,H2O2又可以在铜的催化下生成羟基自由基等活性氧。活性氧容易与植物细胞质膜中的不饱和脂肪酸反应,引起膜脂过氧化,引起过氧化产物丙二醛(MDA)含量的升高。
铜还可与细胞膜蛋白的巯基或磷脂分子层的磷脂类物质反应,改变膜蛋白磷脂结构,透性增大,导致细胞内一些可溶性物质外渗,从而影响物质在生物体中的运输。膜透性可作为植物受害的重要评价指标。Strange等认为铜毒害会导致细胞膜的强度下降,铜渗入细胞内,影响细胞器的结构功能,同时使胞内物质外渗而亏缺。
铜污染还会抑制其他营养元素的吸收,主要是由于铜对根系的伤害和吸收拮抗作用。过量铜会抑制紫云英N、P、K、Zn等养分吸收,茎叶中含量降低,这与铜的投加浓度呈显著负相关,而N含量达极显著负相关水平,一方面是由于过量铜对根系N吸收的抑制,另一方面可能是根瘤形成和固氮受抑的缘故,徐红宁等也指出,铜污染存在下,植物根部生育受阻,细胞结构损坏,细胞膜渗透性提高,使K、P、Oi等离子外渗,植物根部P、K、Ca、Mg、Fe、Na、S等含量趋于降低。
七、土壤铜污染对土壤微生物基础呼吸及土壤酶的影响
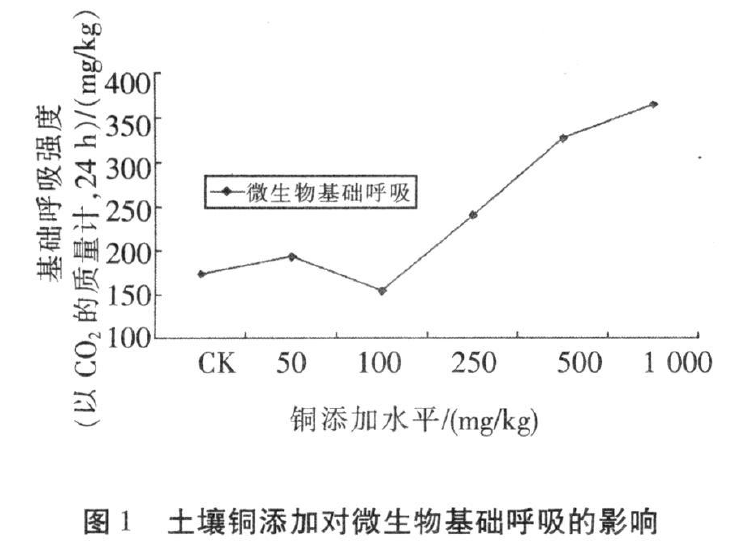
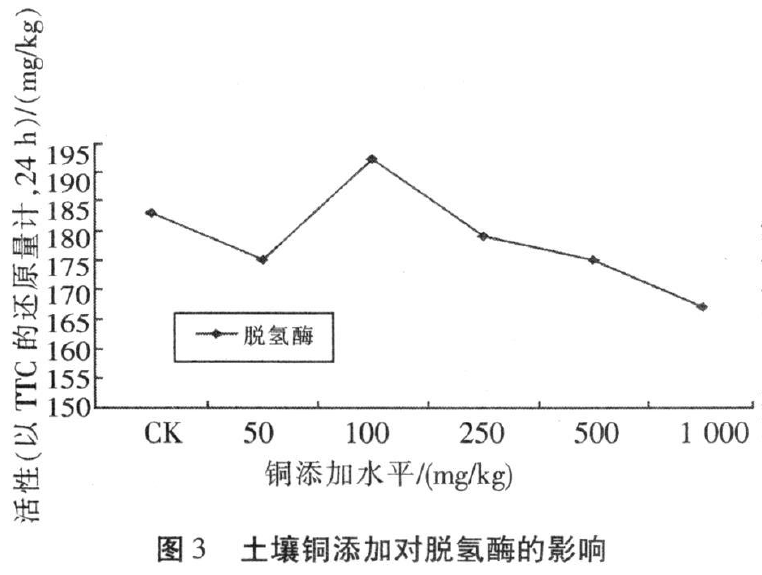
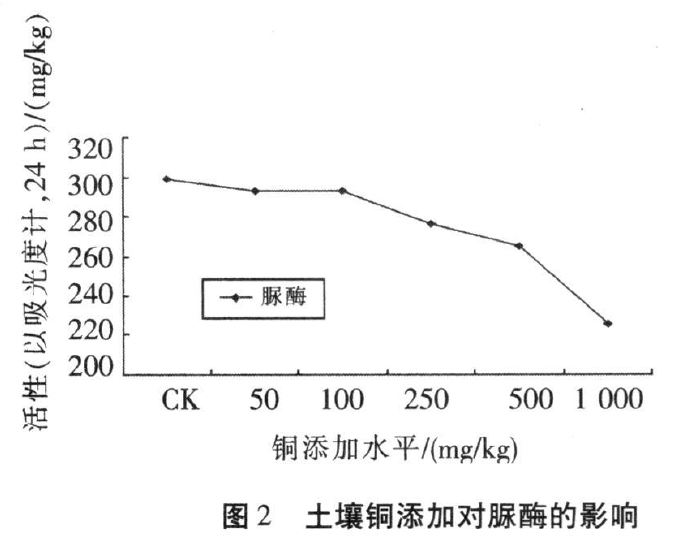
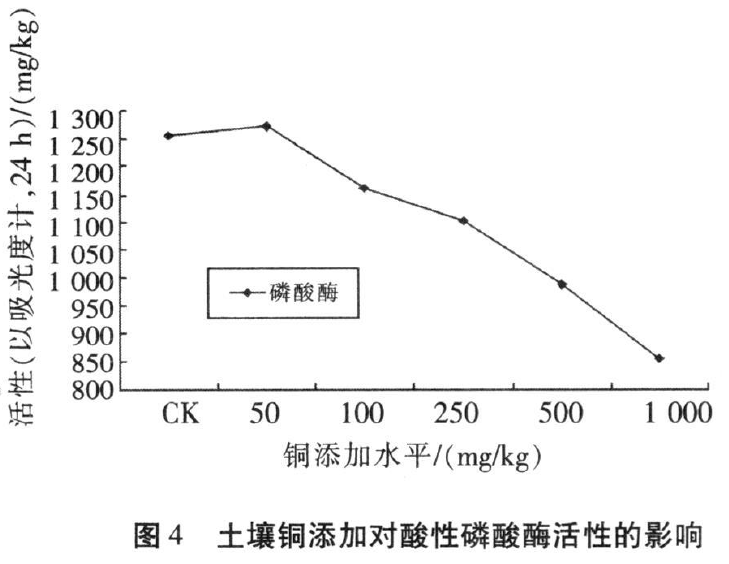
通过室内培养试验,研究了土壤铜污染对土壤微生物基础呼吸及土壤脲酶、脱氢酶、酸性磷酸酶的影响。结果表明,土壤微生物基础呼吸在低水平铜(≤100mg/kg)添加下呈现出先上升后下降的趋势,而随着土壤铜添加水平的进一步提高(>100mg/kg),微生物基础呼吸作用迅速增强;土壤脲酶则随着铜含量的增加呈现出不断下降趋势,土壤磷酸酶活性则在低水平下上升,而随着添加水平的进一步提高迅速降低。可见,这两种酶对土壤铜毒害反应灵敏,可作为土壤铜污染评价的指标;而土壤脱氢酶则对铜含量的变化没有表现出明显的统计规律性,不适宜作为土壤铜污染评价的酶学指标。
沈桂琴等的研究显示重金属对土壤脲酶、转化酶、磷酸酶和蛋白酶活性有明显的抑制作用,同时发现“抗性酶活性” 现象,认为当重金属在土壤中达到一定水平时,大部分微生物死亡,而一小部分微生物在有毒物质污染下能生存下来,自行繁殖,从而产生抗性酶活性,表观上酶活性值降低后又增大,有时还会出现多个抗性峰。如本研究中的土壤磷酸酶在铜添加水平为50mg/kg的时候出现了一次抗性峰,而土壤脱氢酶分别在铜添加水平在100mg/kg时出现一次抗性峰。
八、铜污染土壤的修复技术
对于铜污染土壤的修复和其它重金属污染土壤的修复技术相同,都有物理、化学和生物3大类,物理方法投入大,化学方法难持久,对大面积土壤污染更是由于成本太高而无法实施。与之相比,植物修复是一种投资少、能持久、适宜大面积污染治理的一种方法。自1983年,Chaney提出了利用超富集植物清除土壤中重金属污染的思想,即植物修复(phytoremediation),有关超积累植物的研究日益增多。迄今为止,已发现铜超积累植物有海州香薷(Elsholtzia haichowensis)、星香草(Haumaniastrum robertii)、紫花苜蓿等。其中异叶柔花(Aeollanthus biformifolius)含铜量高达13500μg/g,是已知的铜积累量最高的植物。在植物对铜的耐性中,细胞壁起着重要作用,其次是叶绿体。通过种植铜超富集植物,能有效地将铜从土壤中取出,达到修复目的。近年来,人们在植物修复的同时,通过在土壤中接种蚯蚓或添加螯合剂(EDTA、DTPA、HEDTA、NTA等)等方式,使被土壤固相键合的重金属重新释放并进入土壤溶液,增强土壤中重金属的生物有效性,继而提高植物修复效率。已经取得显著效果。
1、植物修复试验
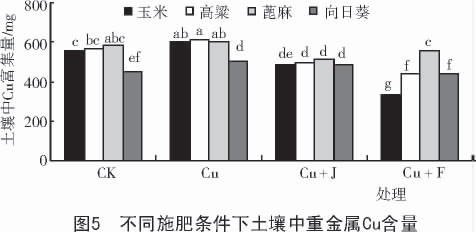
为了研究植物对重金属Cu 污染土壤的修复作用,采用盆栽试验,在不同的施肥条件下,对玉米、蓖麻、高粱、向日葵4 种作物成熟期根、茎、叶、穗中Cu 的富集量以及修复后土壤中重金属Cu 的含量进行测定。结果表明,对于玉米、高粱、向日葵3 种作物来说,最好的修复方式是施腐殖酸(F),而蓖麻最好的施肥方式是施菌肥(J);4 种作物对重金属Cu 富集量从高到低依次为:玉米>高粱>向日葵>蓖麻,相应地土壤中剩余的重金属Cu 含量从高到低依次为:蓖麻>向日葵>高粱>玉米。
试验共设4 个处理,分别为:空白(CK);铜处理土壤(Cu);铜处理土壤+ 腐殖酸(Cu+F);铜处理土壤+ 菌肥(Cu+J)。在4 种处理的土壤上种植4 种作物,重复3 次。每盆装10 kg 的供试土壤,经测定土壤中重金属铜含量为25.835 m g/kg,每盆再施用CuCl2·2H2O(分析纯)1.993 1 m g,土壤重金属铜含量达到100 m g/kg(Cu 污染达到二级标准),加腐殖酸(或菌肥)处理为每10 kg 土壤施加5 g。
2、改良剂修复试验
以一次性添加木炭、石灰和磷灰石稳定化修复4 年后的土壤为研究对象(土壤表层0-17cm均匀混入,磷石灰1.48吨/亩;石灰0.3吨/亩;木炭4.46吨/每亩),探讨了土壤中铜镉有效性和土壤微生物群落结构的变化。结果表明,3种改良剂的添加提高了土壤pH 值,降低了土壤交换性酸和交换性铝的含量,使铜镉由活性态向非活性态和潜在活性态转化,其中磷灰石和石灰的处理效果优于木炭处理。表明改良剂处理后增加了土壤微生物对碳源的利用能力,提高了其功能多样性。PCR-DGGE分析结果显示,改良剂处理后土壤细菌优势群的数量显著增加,木炭、石灰和磷灰石处理Shannon 指数分别比对照提高了0.22、0.39 和0.24。相关性分析表明,土壤酸度和重金属有效性是影响稳定化修复重金属污染土壤细菌结构多样性差异的主要因素。

土壤重金属活性的降低可能是由于改良剂显著提高了土壤pH 值,这有助于提高粘土矿物、有机质和铁锰氧化物等变价胶体的负电荷,增加土壤对重金属的吸附能力。另外,Bolan 等也发现石灰的添加促进了活性Cu 向非活性和潜在活性形态转变。石灰对Cu 和Cd 的固定主要涉及形成碳酸盐或氢氧化物沉淀以及离子交换等。对于磷灰石来说,其对Cu 和Cd 的固定主要通过表面络合、共沉淀、离子交换和固体的溶解作用等。如Shahid 等研究表明溶解性磷和固体性磷材料均能有效降低土壤中Pb 和Cd 的生物有效性。木炭对Cu 和Cd 的固定主要通过吸附、络合和离子交换等方式。
重金属污染土壤的修复不仅仅在于土壤重金属总量及有效性的降低,土壤生物多样性的恢复也是一个重要的方面。微生物是土壤最活跃的组成,大量研究表明,土壤微生物对重金属污染物的响应十分敏感。因为重金属在土壤微生物的生命过程中扮演重要的角色,如Co、Cu、Mn、Zn 和Ni 等是微生物生长的必需元素,它们在微生物生化反应中起到催化作用,对蛋白质结构和细胞壁具有保护功能,并参与一些氧化还原过程。另外,当土壤中存在较高浓度的重金属时,对土壤微生物会产生显著的效应:一是不适应新环境的微生物数量的减少或绝灭;二是适应新环境的微生物数量的增加和积累。因此,土壤长期遭受重金属污染后,土壤微生物的群落结构、微生物数量、土壤酶活性可能发生显著的变化。如李小林等研究表明四川省汉源县福泉乡万顺铅锌矿区尾矿区(DTPA 提取态Zn、Pb 和Cd含量分别为790、883 和8mg/kg)比对照(DTPA提取态Zn、Pb 和Cd 含量分别为16、8 和1mg/kg)中细菌、真菌和放线菌数量分别降低了98.6%、92.2%和99.0%。
3、改良剂修复试验2
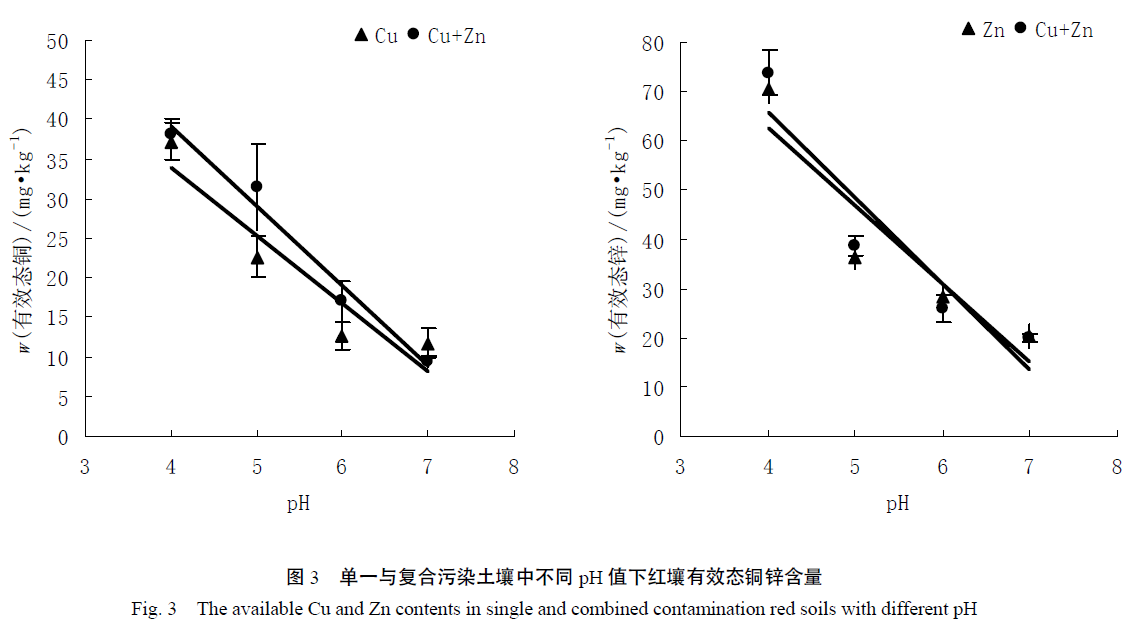
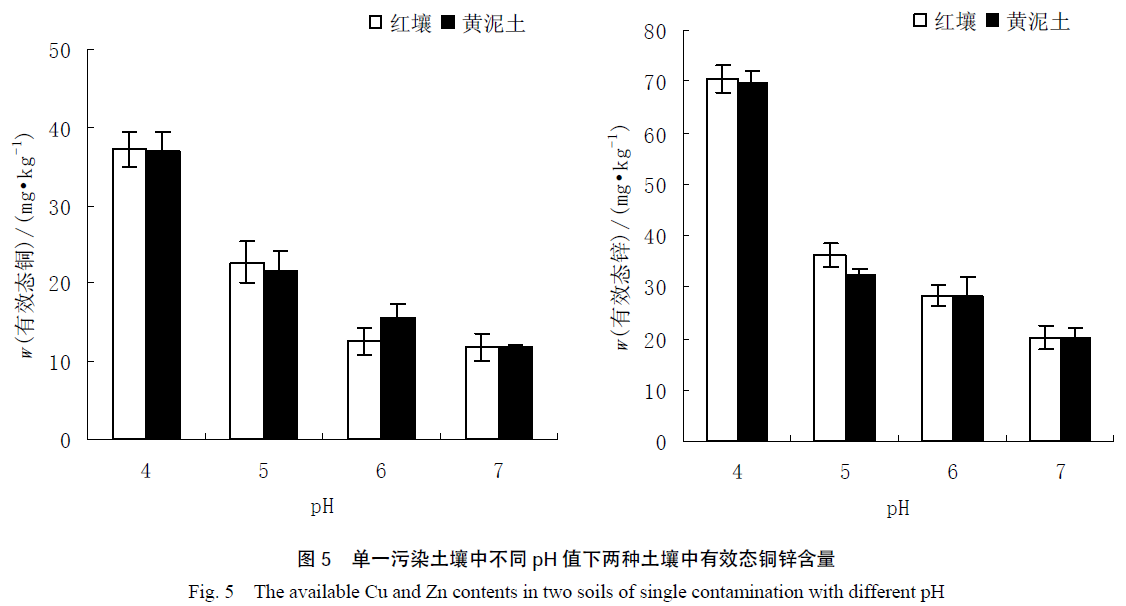
在红壤与黄泥土中施用石灰、重钙和沸石,观测土壤有效态铜锌含量及pH,并测定了不同pH 值下土壤有效态铜锌含量,以阐明改良剂影响土壤重金属有效性的机理。向供试土壤中外源加入一定量的铜锌溶液,制成铜、锌污染土壤,稳定平衡30 d,采用CaCl2 浸提法测定土壤有效态铜锌的含量。结果表明,施用改良剂能显著降低土壤铜锌的有效性,其中石灰的效果最佳,沸石次之,重钙最差。两种土壤中,复合污染下铜锌有效态含量均高于单一污染,其中铜单一污染有效态含量与复合污染差异显著(P0.05)。可能是因为锌比铜竞争力更强,更易于被土壤吸附固定。随着土壤pH 升高,两种土壤的有效态铜锌含量均显著下降,且复合污染高于单一污染;而在相同pH 值下,两种土壤中有效态铜锌含量的差异不显著。可见,pH 值是影响土壤重金属有效性的关键因素。改良剂影响土壤重金属有效性的主要机理在于其能显著提高土壤pH 值,致使有效态重金属含量明显下降。
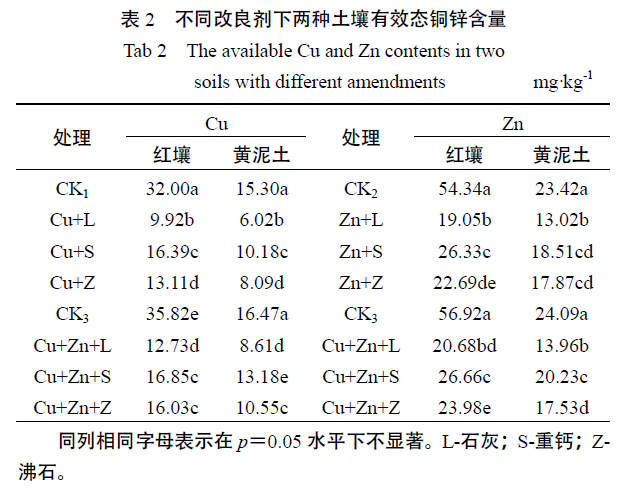
试验选用三种改良剂,石灰、重钙和沸石,施入量分别为2.50 g/kg、4.00 g/kg和9.00 g/kg。红壤施用石灰,pH 平均提高2.1 个单位,施用重钙和沸石pH 平均提高1.7-1.8 个单位。黄泥土施用石灰、重钙和沸石,pH 平均提高0.8、0.5和0.6 个单位。三种改良剂,石灰对土壤pH 的增幅作用最大、沸石次之、重钙最小。
参考文献:
黄国勇等. 根际与非根际土壤铜化学行为的研究进展。中国农业科技导报,2014,16(2):92-99
刘斌等. 广西耕地土壤铜的含量及其影响因素。广西农业科学 2006年第37卷第6期
叶云山. 铜对蔬菜的毒害效应及土壤铜临界值研究
贾彦博等. 土壤铜污染的微生物及酶学指标研究。广东微量元素科学2009年第16卷第3期
荆林晓等. 土壤铜污染的影响因素及其修复技术研究。环境科学与管理第33卷第10期
李文庆等. 有机肥对土壤铜形态及其生物效应的影响。水土保持学报,2011年第25卷第2期
郭卓杰等. 不同施肥条件下不同作物对重金属土壤铜的修复效果及作用。山西农业科学2013,41(11):1209-1211
崔红标等. 改良剂对土壤铜镉有效性和微生物群落结构的影响。中国环境科学 2016,36(1):197-205
王宝奇等. 改良剂对中国两种典型土壤铜锌有效性的影响及机理。生态环境 2007, 16(4): 1139-1143








